La vita di un bambino viene salvata con la terapia genica personalizzata
Medicina genetica di precisione: da un caso a un modello riproducibile
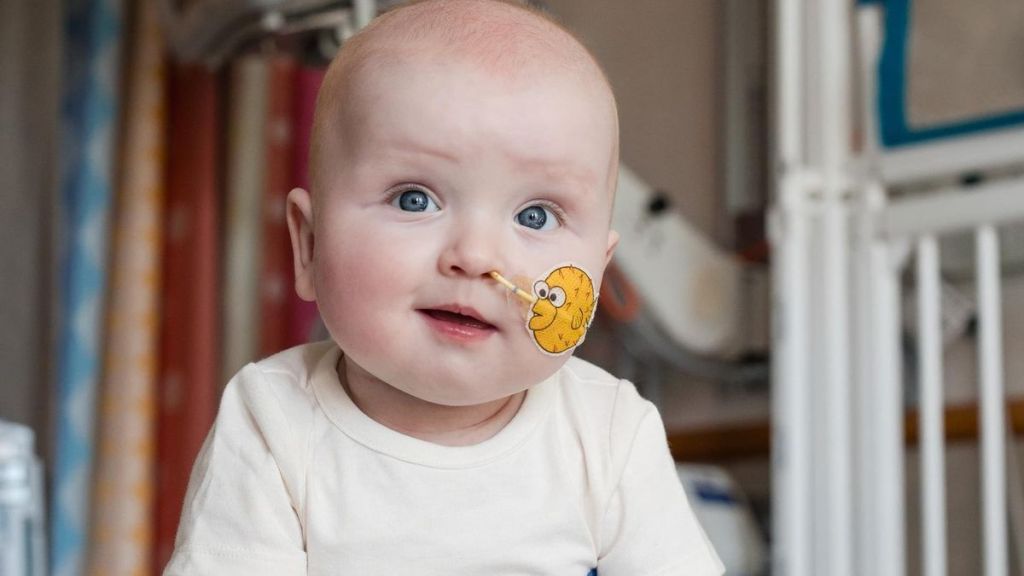
Un gruppo di ricercatori provenienti da diversi paesi, in quella che può essere definita un’impresa senza precedenti, è riuscito a sviluppare, in soli sei mesi, una terapia genica per un singolo paziente: un neonato di nome KJ Muldoon, salvandogli così la vita. Questo trattamento si basava su una tecnica chiamata editing di base ed era in grado di correggere la mutazione genetica che causava una grave malattia metabolica.
Questo caso ha aperto un nuovo campo nella medicina di precisione, che consiste nella creazione di nuove terapie genetiche personalizzate che potrebbero essere efficaci nel trattamento di altre malattie rare, attualmente incurabili, e in tempi record.
Il caso che ha dato inizio a tutto
La mutazione CPS1 con cui KJ è nato impedisce la produzione di un enzima epatico necessario per eliminare l’ammoniaca. L’accumulo di questa sostanza nel sangue può portare a danni cerebrali e persino alla morte.
Finora, il trapianto di fegato era l’unico trattamento noto, ma non sempre era possibile. Tuttavia, Rebecca Ahrens-Nicklas del Children’s Hospital di Philadelphia e Kiran Musunuru, cardiologo dell’Università della Pennsylvania, hanno implementato un nuovo metodo: la terapia genica personalizzata per correggere la mutazione che affliggeva KJ.
Per raggiungere questo obiettivo, hanno utilizzato l’editor genetico CRISPR-Cas9 in una versione avanzata chiamata editor di base, e in questo modo sono stati in grado di modificare una singola “lettera” del DNA nel gene difettoso. Questa piccola modifica è stata sufficiente a ripristinare la funzionalità del gene e ha permesso all’organismo di KJ di produrre normalmente l’enzima CPS1.
L’effetto è stato sorprendente. KJ ha ricevuto la terapia innovativa e i suoi livelli di ammoniaca sono diminuiti, mentre allo stesso tempo il suo sviluppo è tornato normale, consentendogli di ridurre la dose abituale di farmaci. Attualmente, KJ mangia cibi solidi, impara a stare in piedi e muove i primi passi. Sua madre, Nicole Aaron, riassume con entusiasmo: “Celebriamo ogni piccolo traguardo; ha una luce che illumina qualsiasi stanza”.
La stessa strategia; altri pazienti
Il successo ottenuto con la cura di KJ ha portato molte famiglie, i cui membri soffrono di malattie rare, a chiedersi se questa opportunità arriverà presto.
Gli stessi professionisti sanitari che hanno curato KJ stanno pianificando una sperimentazione clinica che coinvolgerà tra 5 e 15 partecipanti affetti da mutazioni che impediscono la normale elaborazione dell’ammoniaca.
La caratteristica di questo nuovo lavoro è la sua somiglianza con il precedente, poiché manterrà gli stessi componenti dell’editor di base e cambierà solo l’RNA guida, che lo indirizza nel punto in cui si trova la mutazione specifica di ogni persona.
Questo sistema consentirà di fornire altri trattamenti personalizzati in tempi più rapidi (circa 3-4 mesi) e a costi inferiori. Inoltre, la Food and Drug Administration (FDA) statunitense ha deciso di validare, per i nuovi partecipanti, i dati di sicurezza relativi alla terapia genica applicata a KJ. Ciò ridurrà il numero di sperimentazioni.
Nuovo quadro normativo
Finora, la FDA richiedeva che ogni nuova proposta di terapia genica fosse sottoposta a un lungo processo normativo e a una sperimentazione clinica separata, anche se le differenze rispetto ad altri trattamenti erano minime. Attualmente, con l’avvento di questo tipo di terapia personalizzata, questo requisito è in fase di revisione.
Per questo motivo, i ricercatori hanno deciso di pubblicare la loro corrispondenza con la FDA. In questo modo, altri team di ricerca che sviluppano trattamenti simili avranno a disposizione linee guida che faciliteranno il loro lavoro. “Vogliamo che il nostro lavoro sia uno tsunami che sollevi tutte le barche”, ha commentato Fyodor Urnov, uno dei pionieri dell’editing genetico presso l’Institute for Innovative Genomics dell’Università della California, Berkeley.
Se questo modello andasse avanti, potrebbe dare inizio a una nuova era, con terapie progettate su richiesta e in base alle caratteristiche genetiche di ciascun paziente, e al contempo inserite in modelli normativi rapidi ma sicuri.
L’apogeo della medicina personalizzata
L’aumento della terapia personalizzata non si limita al lavoro oggetto di questo articolo, poiché diverse istituzioni hanno recentemente segnalato progetti simili.
Il CRISPR Pediatric Cures Center, una collaborazione tra l’Università della California, Berkeley, e l’Università della California, San Francisco, mira ad accelerare lo sviluppo di terapie geniche personalizzate. L’Agenzia per i Progetti di Ricerca Avanzata sulla Salute (HARPA) del governo statunitense sta inoltre finanziando due programmi incentrati sullo sviluppo e l’implementazione della medicina genetica di precisione.
“Ora sono più ottimista di quanto non lo fossi in passato”, afferma Joseph Hacia, genetista medico presso la Keck School of Medicine dell’Università della California del Sud a Los Angeles.
Sfide
Nonostante l’entusiasmo sia palpabile, restano ancora enormi sfide. Sono necessarie attrezzature complesse, rigorosi processi di controllo qualità e laboratori ad alta sicurezza. L’implementazione di una terapia personalizzata è estremamente costosa.
È inoltre necessario considerare l’equità affinché tutti possano accedere a questi trattamenti. Gli scienziati sono fiduciosi che, con la standardizzazione dei componenti comuni e la semplificazione dei quadri normativi, i costi diminuiranno e l’accesso aumenterà.
Il ruolo delle aziende biotecnologiche sarà fondamentale per realizzare modelli di business sostenibili che portino a trattamenti personalizzati, mantenendone al contempo la sicurezza e l’efficacia.
Una terapia su misura
Supponendo che la sicurezza e l’efficacia di questi studi siano confermate e che la FDA approvi un trattamento dopo averlo testato su soli 10 o 15 partecipanti, otterremmo quella che potremmo definire una nuova classe di terapie geniche rapide, personalizzate e scalabili: entreremmo in un mondo finora inimmaginabile.
“I trattamenti personalizzati sono sicuramente la direzione che dobbiamo seguire”, afferma Ryan Maple, direttore esecutivo della Global Foundation for Peroxisomal Disorders di Tulsa, Oklahoma. E conclude: “Questa tecnologia potrebbe essere più di una semplice svolta. Potrebbe essere rivoluzionaria”.
Il confine tra ricerca e pratica clinica può diventare molto sottile quando, come nel caso di KJ, l’urgenza si allinea all’innovazione biotecnologica. Lungo questo lungo percorso della scienza, potremmo dire che alcuni progressi biomedici vengono conseguiti lettera per lettera (del DNA).
 (EN)
(EN)
 (ES)
(ES)
 (IT)
(IT)





